Agar dapat memahami ikatan kimia, Anda harus mampu membandingkan proses pembentukan ikatan ion, ikatan kovalen, ikatan koordinasi, dan ikatan logam serta hubungannya dengan sifat fisika senyawa yang terbentuk.
Materi Pelajaran Kimia Kelas X, Semester 1. Oleh : Gianto,SPd
Atom memiliki kecenderungan untuk mencapai kestabilan dengan cara berikatan dengan atom lain. Elektron yang berperan pada pembentukan ikatan kimia adalah elektron valensi dari suatu atom/unsur yang terlibat. Salah satu petunjuk dalam pembentukan ikatan kimia adalah adanya golongan unsur yang stabil yaitu golongan VIIIA atau golongan 18 (gas mulia). Oleh sebab itu dalam pembentukan ikatan kimia, atom-atom akan membentuk konfigurasi elektron seperti pada unsur gas mulia.
Unsur gas mulia mempunyai elektron valensi sebanyak 8 (oktet) kecuali Helium 2 (duplet), seperti terlihat pada table di bawah ini.
| Periode | Unsur | Nomor Atom | K | L | M | N | O | P |
| 1 | He | 2 | 2 | |||||
| 2 | Ne | 10 | 2 | 8 | ||||
| 3 | Ar | 18 | 2 | 8 | 8 | |||
| 4 | Kr | 36 | 2 | 8 | 18 | 8 | ||
| 5 | Xe | 54 | 2 | 8 | 18 | 18 | 8 | |
| 6 | Rn | 86 | 2 | 8 | 18 | 32 | 18 | 8 |
Kecenderungan unsur-unsur untuk menjadikan konfigurasi elektronnya sama seperti gas mulia terdekat dikenal dengan istilah Aturan Oktet. Untuk mengilustrasikan ikatan kimia dapat dilakukan dengan menuliskan rumus Lewis dan rumus ikatan.
Ikatan kimia dibedakan menjadi 4 yaitu :
Ikatan kovalen terdiri dari :
- Ikatan kovalen tunggal
- Ikatan kovalen rangkap dua
- Ikatan kovalen rangkap tiga
- Ikatan kovalen polar
- Ikatan kovalen non polar
Contoh Ikatan Kovalen, lihat gambar di bawah ini !
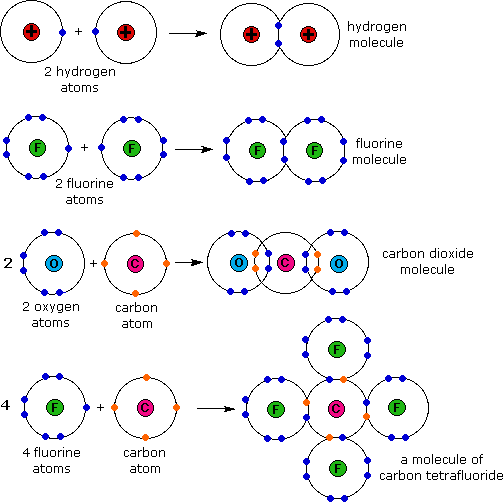
Untuk bahan belajar, silahkan download materi ikatan kimia dari 3 buah buku BSE berikut ini :
Untuk menghadapi tes atau ulangan harian tentang ikatan kimia, silahkan download soal-soal berikut ini sebagai latihan.
- Latihan soal ikatan kimia (PDF) > download







Tidak ada komentar:
Posting Komentar